引言
氟醚菌酰胺,英文通用名为fluopimomide,CAS登记号1309859-39-9,分子式为C15H8ClF7N2O2,分子量为416.68,为类白色粉末,无刺激性气味,熔点:115 ~ 118 ℃,蒸汽压:2.3 × 10-6 Pa (25 ℃),密度: 0.801 g/mL. 该化合物的化学名称为N-(3-氯-5- (三氟甲基)吡啶-2-甲基)-2,3,5,6-四氟-4-甲氧基苯甲酰胺,是山东中农联合生物科技股份有限公司(中农联合)与山东农业大学合作于2010年创新合成的一种新型含氟苯甲酰胺类杀菌剂,也是中农联合第一个商品化的新化合物[1].氟醚菌酰胺能够有效地防止马铃薯晚疫病[2,3]、葡萄霜霉病[4]、辣椒疫霉病[5,6],对番茄灰霉病菌也有较高的抑制活性[7,8],此外氟醚菌酰胺对根结线虫有一定抑制效果[9,10].
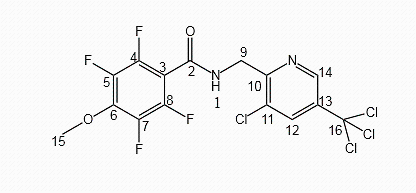
目前,大多数文献主要关注氟醚菌酰胺的合成制备[11]、配方研制[12],而对于其波谱学全归属方面的研究未见报道.对重要药物分子做波谱学全归属不仅对药物生产过程中的质量管控有着非常重要的意义,还为其类似物的合成提供了重要参考,近几年很多文献都做了这方面的研究[13,14].基于此,本文对氟醚菌酰胺的四大波谱数据进行了全归属,测定了氟醚菌酰胺的高分辨率质谱(HR-MS)、红外吸收光谱(IR)、紫外吸收光谱(UV)、核磁共振氢谱(1H NMR)、碳谱(13C NMR)、无畸变极化转移增强谱(DEPT)、同核位移相关谱(1H-1H COSY)、异核单量子相关谱(1H-13C HSQC)、异核多键相关谱(1H-13C HBMC),详细分析了该化合物的1H NMR和13C NMR谱图,并借助二维谱图提供的H-H及H-C键偶合信息,对其信号进行了全面归属.同时,探讨了紫外吸收光谱中各吸收带的意义,以及红外吸收光谱中官能团的振动形式.这些研究结果为氟醚菌酰胺的进一步深入研究提供了重要参考依据.氟醚菌酰胺的化学结构如图1所示.
图1
1 实验部分
1.1 样品与试剂
氟醚菌酰胺标样(97%)购自北京乐研科技股份有限公司,氘代氯仿(CDCl3,氘代率99.8%)购自美国剑桥同位素实验室(CIL)公司.
1.2 仪器和测试条件
称取97%的氟醚菌酰胺标样20 mg,溶于0.5 mL的氘代氯仿中,充分溶解后将其转移至5 mm标准NMR样品管内,之后测定1H NMR、13C NMR、DEPT-90、DEPT-135、1H-1H COSY、1H-13C HSQC、1H-13C HMBC谱图.以TMS为内标(δH 0,δC 0),1H NMR和13C NMR的工作频率分别为600.13 MHz和150.95 MHz,实验温度为25 ℃,谱宽分别为12 376.24 Hz和35 971.22 Hz.二维谱包括2D梯度场1H-1H COSY、1H-13C HSQC、1H-13C HMBC谱,均采用标准脉冲程序.1H-1H COSY的F2(1H)和F1(1H)维的谱宽均为9 002.01 Hz,采样数据点阵t2×t1 = 2 048×128,累加次数32;HSQC的F2(1H)和F1(13C)维的谱宽分别为9 002.01 Hz和37 730.23 Hz,采样数据点阵t2×t1 = 1 024×256,累加次数18;HMBC的F2(1H)和F1(13C)维的谱宽分别为8 992.81 Hz和37 730.23 Hz,采样数据点阵t2×t1 = 4 096×128,累加次数32.核磁共振1H NMR、 13C NMR、DEPT、1H-1H COSY、1H-13C HSQC、1H-13C HMBC谱图的信号采集均使用Bruker Avance 600 MHz NMR波谱仪并采用反向三共振TXI探头,数据采集及处理均在Bruker Topspin 2.1系统上完成.紫外光谱用岛津UV-2600紫外光谱仪测定;红外光谱用Vector 33型红外光谱仪(瑞士Bruker公司)测定;高分辨质谱采用AB SCIEX Triple Quad 5500(美国AB SCIEX公司),离子源为EI.
2 结果与讨论
2.1 氟醚菌酰胺质谱分析
如图2所示,采用高分辨质谱技术对氟醚菌酰胺进行分析,在负离子模式下观察到m/z值为415.007 1(35Cl)的准分子离子峰[M-H]-,与理论值415.008 4一致.其同位素峰m/z值为417.004 4(37Cl),理论值为417.005 5.同时检测到多个特征性碎片峰.这些质谱数据与氟醚菌酰胺的理论分子量相符,证实了样品的分子结构特征.
图2
2.2 氟醚菌酰胺紫外吸收光谱分析
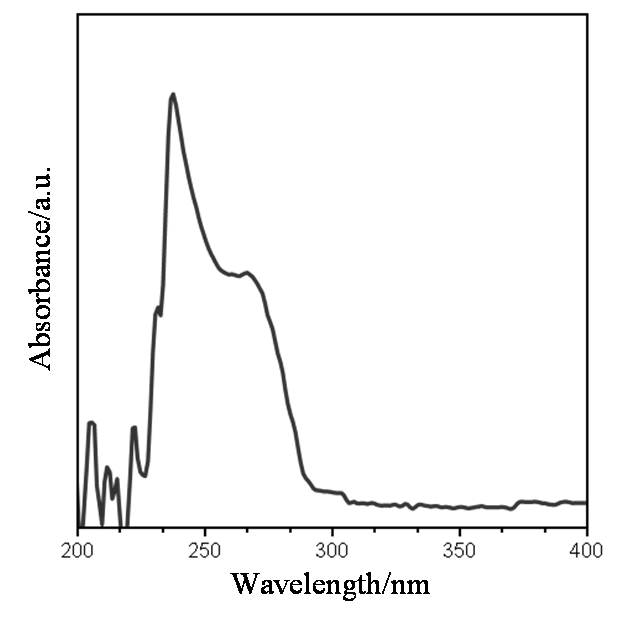
如图3所示,氟醚菌酰胺在四氢呋喃溶液中的紫外吸收光谱图在230~290 nm附近有较强的吸收带,吸收峰(λmax = 237 nm)为B吸收带,谱图分析表明,该化合物分子骨架中含有芳香环体系,这一结构特征与氟醚菌酰胺的结构相符.
图3
2.3 氟醚菌酰胺红外吸收光谱分析
如图4所示,在红外吸收光谱中,3 290 cm-1处有较强的吸收峰,是由N-H的伸缩振动造成的特征吸收峰,且1 560 cm-1为N-H面内弯曲振动;2 845 cm-1处的吸收峰为饱和碳原子-CH3上的C-H伸缩吸收峰;1 686 cm-1处的强吸收峰为C=O的伸缩振动,表明分子存在醛、酮、酰胺等结构;3 030 cm-1附近的两个吸收峰,峰强度较弱,为C-H的伸缩振动引起,是芳香烃的特征吸收峰,这说明结构中有芳香烃的存在,且1 493 cm-1、1 506 cm-1及1 588 cm-1为芳香烃的C=C骨架振动或者C=N伸缩振动;1 229 cm-1和 1 330 cm-1位置出现的显著吸收峰可归因于C-F键引起的伸缩振动,这种特征通常出现在单个碳原子上连接多个氟原子的结构单元中.基于这一光谱特征,可以推断该化合物分子中可能存在三氟甲基(-CF3)官能团.
图4
2.4 氟醚菌酰胺核磁共振分析
图5
图6
图6
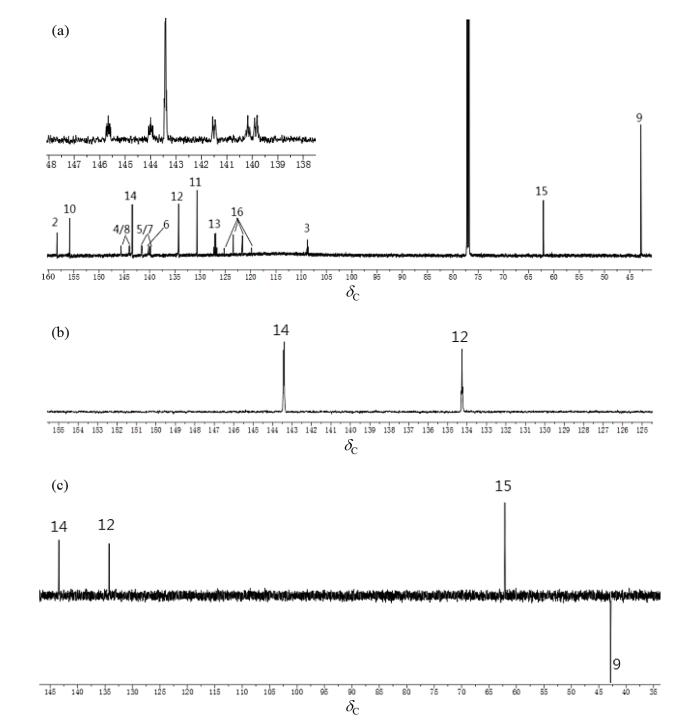
氟醚菌酰胺(a) 13C NMR谱、(b) DEPT-90和(c) DEPT-135谱图
Fig. 6
(a)13C NMR, (b) DEPT-90 and (c) DEPT-135 spectrum of fluopimomide
图7
图8
图9
图9
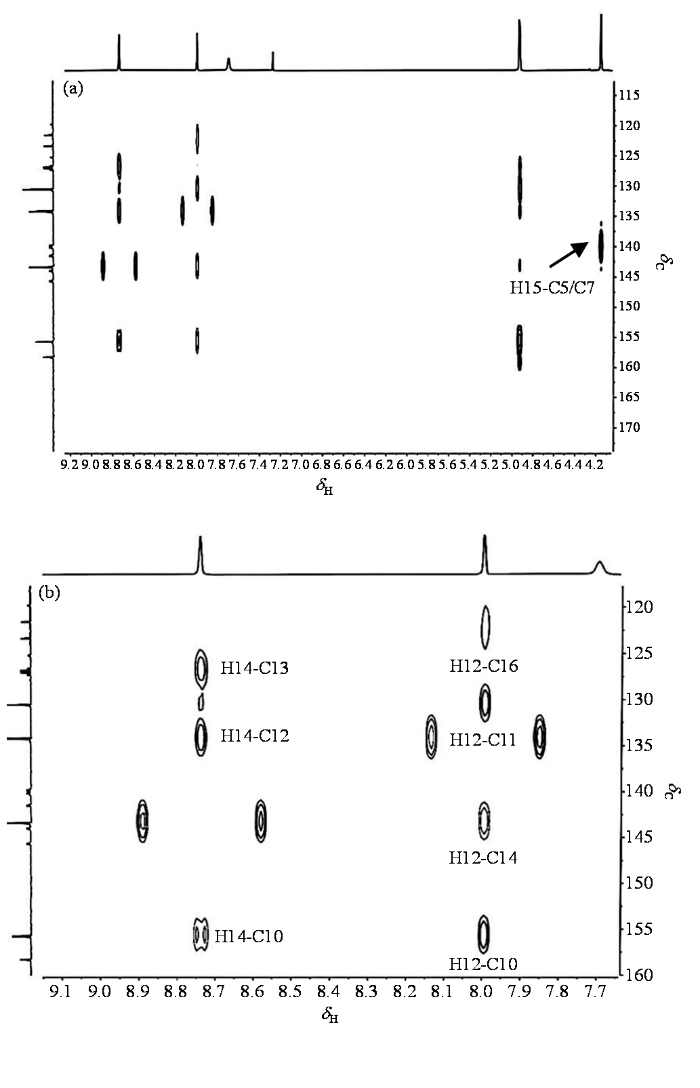
氟醚菌酰胺1H-13C HMBC谱图(a)及其局部放大图(b)
Fig. 9
1H-13C HMBC spectrum of fluopimomide (a) and its partial enlargement (b)
表1 氟醚菌酰胺核磁共振信号全归属
Table 1
| Position | δC (J/Hz) | δH (J/Hz) | HSQC | 1H-1H COSY | HMBC |
|---|---|---|---|---|---|
| 1 | / | 7.68 (s, 1H) | / | H-9 | / |
| 2 | 158.3 | / | / | / | / |
| 3 | 108.7 (t, J = 17.6 Hz) | / | / | / | / |
| 4, 8 | 144.8 (dd, J = 251.4 Hz;17.6Hz) | / | / | / | / |
| 5, 7 | 140.7 (dd, J = 265.7 Hz;15.4Hz) | / | / | / | H-15 |
| 6 | 140.2 (t, J = 11.0 Hz) | / | / | / | / |
| 9 | 42.8 | 4.92 (s, 2H) | / | H-1 | / |
| 10 | 155.8 | / | / | / | H-9, H-12, H-14 |
| 11 | 130.6 | / | / | / | H-9, H-12 |
| 12 | 134.3 (q, J = 1.8 Hz) | 7.98 (s, 1H) | + | H-14 | H-14 |
| 13 | 127.0 (q, J = 33.8 Hz) | / | / | / | H12, H-14 |
| 14 | 143.4 (q, J = 1.6 Hz) | 8.72 (s, 1H) | + | H-12 | H-12 |
| 15 | 62.1 | 4.14 (s, 3H) | + | H-15 | / |
| 16 | 122.4 (q, J = 272.9 Hz) | / | / | / | H-12 |
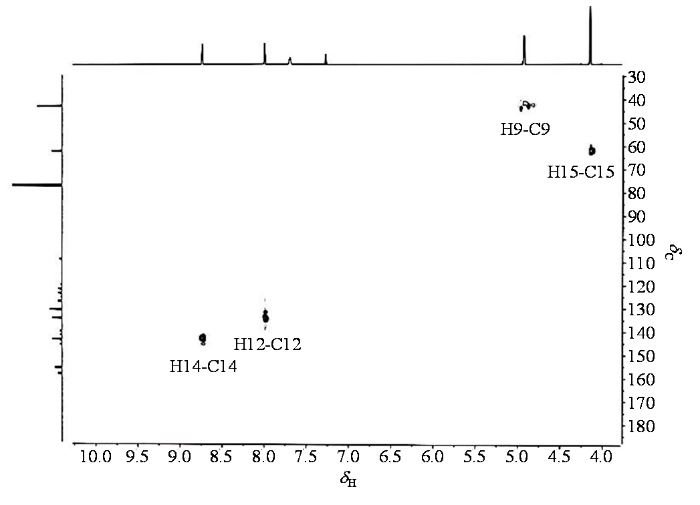
1H NMR(图5)中最高场的单峰δH 4.14 (s, 3H),根据其化学位移、积分面积及DEPT-90与DEPT-135(图6)给出的信息可以归属为甲氧基上的三个化学环境相同的氢原子信号H-15,同时由于1H-1H COSY(图7)谱中未观察到δH 4.14 (s, 3H)与其他质子信号的相关峰,进一步佐证了δH 4.14 (s, 3H)为H-15原子的信号,根据HSQC(图8)谱中与δH 4.14 (s, 3H)相关连的碳原子为δC 62.1,可以把δC 62.1归属为C-15. 1H NMR谱中第二高场信号δH 4.92 (s, 2H)也较好归属,根据其化学位移、积分面积以及DEPT-90与DEPT-135给出的信息可以归属它为H-9原子所对应的信号,根据HSQC谱中与δH 4.92 (s, 2H)相关联的碳原子为δC 42.8,可以确定与H-9原子相连的碳原子为C-9(δC 42.8),再根据1H-1H COSY谱中H-9与δH 7.68 (s, 1H)相关,因此将δH 7.68 (s, 1H)归属为H-1原子所对应的信号.由吡啶环的化学位移可知,与氮原子相邻的氢原子应受氮原子的影响会在较低场[15],故可将δH 8.72 (s, 1H)归属为H-14所属氢原子信号,δH 7.98 (s, 1H)归属为H-12所属氢原子信号,同时根据HSQC谱δH 8.72 (s, 1H)与δC 143.4 (q, J = 1.6 Hz)相关联、δH 7.98 (s, 1H)与δC 134.3 (q, J = 1.8 Hz)相关联,可以归属δC 143.4 (q, J = 1.6 Hz)为C-14原子的信号、δC 134.3 (q, J = 1.8 Hz)为C-12原子的信号.
根据HMBC(图9)谱,与亚甲基上氢原子H-9相关的是δC 155.8与δC 130.6,结合氟醚菌酰胺的结构及化学位移,可以归属δC 155.8的季碳信号为与C-9相连的C-10信号,而δC 130.6的季碳原子信号为吡啶环上与C-10相连的C-11.氢原子H-14与δC 127.0 (q, J = 33.8 Hz)、δC 134.3、δC 155.8有远程相关,已知δC 134.3为C-12的信号,δC 155.8为季碳C-10的信号,由此可以确定δC 127.0 (q, J = 33.8 Hz)为吡啶环上与C-14碳原子相连的C-13所属碳原子信号.氢原子H-12与δC 122.4 (q, J = 272.9 Hz)、δC 130.6、δC 143.4、δC 155.8有远程相关,已知δC 130.6为季碳C-11的信号,δC 143.4为C-14所属信号,δC 155.8为季碳C-10的信号,所以可以确定δC 122.4 (q, J = 272.9 Hz)是与C-13碳原子相连的三氟甲基上的碳原子C-16信号,因为该化合物含有氟原子,故核磁共振碳谱会产生裂分,且随着相隔键数的增加,耦合常数会减小,由此可以验证δC 122.4 (q, J = 272.9 Hz)为三氟甲基上的碳原子C-16信号.
HMBC谱中,与氢原子δH 4.14 (s, 3H)相关联的碳原子为δC 140.7 (dd, J = 265.7 Hz;15.4Hz),由此可以确定δC 140.7 (dd, J = 265.7 Hz;15.4Hz)为与甲氧基远程相关的苯环上的碳原子C-5或者C-7,由于C-5、C-7是处在相同化学环境中的碳原子,且由于自身相连的氟原子与邻碳上相连的氟原子的共同作用,此碳信号被裂分成了多重峰,因此δC 140.7 (dd, J = 265.7 Hz;15.4Hz)为C-5、C-7所共有的碳信号.同理可得,化学位移δC 144.8 (dd, J = 251.4 Hz;17.6Hz)处的碳原子信号为C-4、C-8所共有的碳信号.图9(b)中剩余四个未标注的相关峰,其化学位移与直接1JCH耦合信号相符,为HMBC脉冲序列对直接耦合信号的抑制不完全而产生的.
羰基上碳原子的化学位移一般在150~220 ppm范围内,所以可以确定δC 158.3为羰基中的碳原子信号C-2.剩余两个碳原子的化学位移为δC 140.2 (t, J = 11.0 Hz)、δC 108.7 (t, J = 17.6 Hz),所属碳原子为C-3或者C-6,由于碳原子C-6与氧原子相连,而氧原子会使得与其所连碳原子的化学位移往低场移动,所以碳原子C-6所对应的化学位移为δC 140.2 (t, J = 11.0 Hz),碳原子C-3所对应的化学位移为δC 108.7 (t, J = 17.6 Hz).
3 结论
本文对氟醚菌酰胺进行了四大波谱检测,指出了紫外光谱的特征吸收带、红外光谱的特征吸收峰及其对应的各官能团的振动形式,并且对该化合物的1H NMR和13C NMR以及二维NMR谱的信号进行了全归属.上述波谱学数据证明了氟醚菌酰胺的结构.
利益冲突
无
参考文献
Fluopimomide-A newly developed fungicide in China: recent research progress
[J].
我国自主创制农药氟醚菌酰胺的研究进展
[J].
Synergism and field control effect of mixtures of fluopimomide and iprovalicarb against Phytophthora infestans
[J].
氟醚菌酰胺和缬霉威对马铃薯晚疫病菌增效及田间防效
[J].
Synergistic interaction and field control effect of mixtures of LH-2010A with dimethomorph against Phytophthora infestans
[J].
氟醚菌酰胺与烯酰吗啉混配对马铃薯晚疫病菌增效作用及田间药效
[J].
Determination of separated and joint toxicity and field control effect of fluopimomide and pyraclostrobin against plasmopara viticola
[J].
氟醚菌酰胺和吡唑醚菌酯对葡萄霜霉病联合毒力及田间防效
[J].
Preliminary studies on the action mechanism of the novel fungicide LH-2010A against Phytophthora capsici
[J].
新型杀菌剂氟醚菌酰胺对辣椒疫霉的作用机制初探
[J].
Effects of soil treated fungicide fluopimomide on tomato (Solanum lycopersicum L.) disease control and plant growth
[J].
Evaluation of the reproductive toxicity of fluopimomide in meloidogyne incognita and caenorhabditis elegans
[J].
Evaluating a new non-fumigant nematicide fluopimomide for management of southern root-knot nematodes in tomato
[J].DOI:10.1016/j.cropro.2019.105040 URL [本文引用: 1]
Spectral analysis of fungicide cyflufenamid
[J].
杀菌剂环氟菌胺波谱学数据全归属
[J].
DOI:10.11938/cjmr20160114
[本文引用: 1]

环氟菌胺是一种具有新型母核结构的优秀杀菌剂.该文采用1H NMR、13C NMR、19F NMR、1H-13C HSQC、1H-13C HMBC和1H-15N HMBC等多种核磁共振(NMR)技术,并结合质谱(MS)、紫外光谱(UV)和红外光谱(IR)等方法对环氟菌胺进行了解析,同时对一维核磁共振(1D NMR)波谱数据进行全归属,讨论了UV和IR的吸收峰与该化合物各官能团的对应关系、19F对其1H和13C NMR谱峰的影响,以及MS主要离子碎片的归属和化合物裂解规律.
Spectroscopic data of fluacrypyrim and interpretations
[J].
嘧螨酯波谱学数据全归属
[J].嘧螨酯为一种新型杀螨剂和STAT3激活抑制剂. 该文对嘧螨酯的紫外吸收光谱(UV)、红外吸收光谱(IR)、质谱(MS)、核磁共振氢谱(1H NMR)、核磁共振碳谱(13C NMR)、DEPT谱、1H-1H COSY谱、异核单量子相关谱(HSQC)、异核多键相关谱(HMBC)进行了解析,并对该化合物所有的核磁信号进行了全归属;同时讨论了紫外光谱吸收带位置和吸收强度与该化合物的生色团对应关系、红外光谱特征吸收峰与该化合物的各官能团的对应关系、氟原子(F)对其13C NMR的影响以及质谱离子碎片的归属和化合物的裂解规律. 该研究将为嘧螨酯的结构确证及其他相关研究提供参考.